(Ciencias de Joseleg) (Química) (Lenguaje químico) (Enlace químico) (Ejercicios resueltos) (Introducción) (Generalidades) (Historia) (Enlace químico fuerte) (Enlace químico débil) (Símbolos de Lewis y el octeto) (Energía reticular) (Enlace covalente y su representación) (Enlace covalente polar) (Diferenciando entre iónico y covalente) (Dibujado estructuras de Lewis) (Estados de oxidación, cargas formales y reales) (Resonancia) (Desviaciones del octeto) (Enlace covalente coordinado) (Enlace metálico) (Teoría del enlace de valencia) (Teoría del orbital molecular) (Efecto del enlace químico en los estados de la materia) (Referencias bibliográficas)
El enlace
covalente coordinado es el que tiene lugar cuando el par de electrones a
compartir los suministra un solo de los átomos involucrados. Este enlace es
semi polar, por cuyo motivo se lo llamó a veces dativo, calificativo
inapropiado, ya que en realidad los electrones no son dados, sino compartidos
en forma desigual.
El enlace
covalente coordinado ocurrirá generalmente cuando un átomo posee un par de
electrones no en las antes pero que son altamente electronegativos, por lo que
aprenderán a capturar partículas positivas, especialmente protones ácidos que
provengan ya sea de un ácido o de la autodisociación del agua, lo cual generará
guión de carga positiva.
el grupo de compuestos que está sometido a el enlace covalente coordinado más importante son aquellos que poseen nitrógenos con electrones no enlazados, de los cuales la sustancia tipo con la cual generamos los ejemplos más comunes es el amoniaco:
Cuando se
generó una reacción con un ácido se puede generar una reacción a 2 pasos, en el
primer paso el amoniaco absorbe el protón para transformarse en el ion amonio, y
en el segundo paso absorbe el año negativo original del ácido para convertirse
en un compuesto de coordinación iónico:
Esa reacción puede ser particularmente útil ya que muchos ácidos
manifiestan propiedades covalentes como la volatilidad a presión y temperatura
constante, por lo que convertirlos a un compuesto de coordinación que exhibe
propiedades iónicas evita que éstos se volatilicen en condiciones normales de
presión y temperatura, lo cual los hace más fáciles de almacenar, y transportar.
Eso es particularmente conveniente ya que muchos alcaloides (compuestos
orgánicos que contienen nitrógenos que se comportan como amoniaco), que son los
compuestos activos de muchos medicamentos, son altamente volátiles y por lo
tanto no se podrían almacenar durante largos periodos de tiempo si no se
pudieran convertir a compuestos de coordinación con propiedades iónicas.

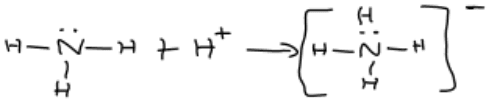

No hay comentarios:
Publicar un comentario